Szabad hozzáférésű komplex természettudományos tananyagok
Fémek rácsszerkezete |
|
Kristálynak nevezzük az olyan szilárd testet, amelynek elemei úgynevezett térrács alakzatot mutatnak. A kristályos anyag részecskéi kristályrácsot alkotnak. A kristály rácspontjaiban található részecskék minősége és a köztük lévő kapcsolat szerint négyféle rácstípust különböztetünk meg:
|
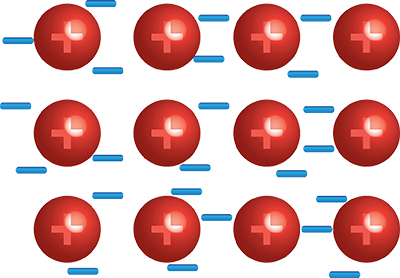 |
A fématomokat kis ionizációs energia, kis elektronvonzó képesség jellemzi, vegyértékelektronjaik könnyen delokalizálódnak. A fémkristályban a rácsban rögzített pozitív töltésű ionokat az elektronok „tengere” veszi körül, az elektronok viszonylag szabadon mozognak a kristályrácsban a pozitív töltések között. |
|
A szabályos, lapon középpontos kockarácsban az elemi cellában az atomok egy kocka csúcsain és a lapok középpontjában vannak. A koordinációs szám 12, azaz 12 másik atom vesz körül egy atomot azonos távolságban: 6 vele egy síkban, alatta és fölötte 3-3. Ez a fématomok legszorosabb illeszkedését biztosítja. Ilyen rácsszerkezetű fémek a legjobban megmunkálhatók: Ag, Au, Al, Ca, Cu, Mn, Ni, Pb, Pd, Pt stb.
|
|
A hatszöges (hexagonális) rácsban a koordinációs szám szintén 12. Az elemi cella egy hatszög alapú hasáb. Ebben a rácsban is szorosan illeszkednek az atomok. Ilyen a kristályrácsa például a következő fémeknek: Be, Mg, Cd, Co, Zn. |
|
|
A térben középpontos kockarácsban az atomok egy kocka csúcsain és annak térközepén helyezkednek el. A koordinációs szám ebben a rácstípusban 8, nem jelenti a legszorosabb illeszkedést a fématomok számára. Térközepes rácsú például a Ba, Cr, Cs, K, Li, Na, Rb, U, V, W.
|
